ICH Q14: desarrollo y gestión del ciclo de vida de ensayos para el control de calidad de acuerdo a los principios Quality by Design
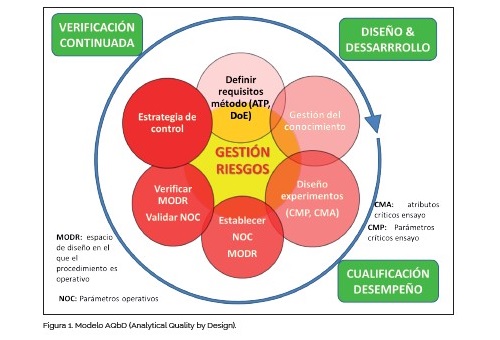
El 1 de abril, la Agencia Europea del Medicamento publicó para su consulta pública el borrador de la Guía ICH Q141 sobre el desarrollo y gestión de su correcto funcionamiento en su ciclo de vida de los procedimientos analíticos (PA, también conocidos como ensayos) utilizados para la evaluación de la calidad de las sustancias y los productos farmacéuticos. El alcance de esta Guía también incluye los PA nuevos o revisados utilizados en los ensayos de liberación y estabilidad de sustanci

